NAD⁺ restaura a memória em modelos da doença de Alzheimer corrigindo erros de RNA
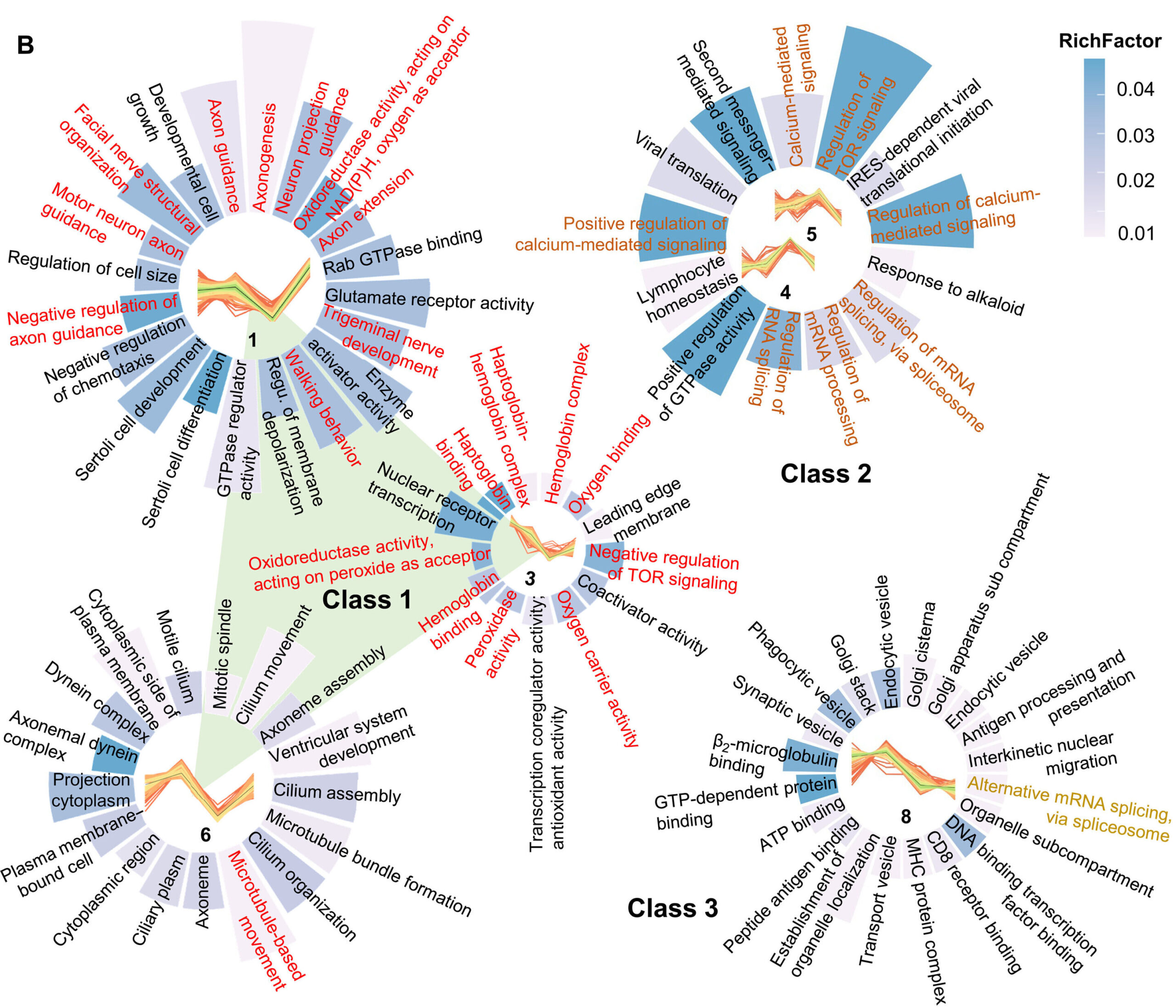
A NR induz a transcrição de genes envolvidos no desenvolvimento de axônios, metabolismo de oxigênio, localização de mitocôndrias e autofagia em camundongos com tauopatia. Termos GO enriquecidos em cada uma das oito classes de clusters em (A); cada gráfico de barras circular representa um cluster ou classe de clusters, e o comprimento da barra se correlaciona com o número de DEGs representados. Os termos GO mostrados em fonte vermelha referem-se ao mRNA. Os clusters 4 e 5 são semelhantes e estão agrupados. A classe 1 inclui os clusters 1, 2 e 6 marcados em vermelho. A classe 2 inclui os clusters 4 e 5 marcados em laranja. A classe 3 inclui o cluster 8 marcado em amarelo. GTPase, guanosina trifosfatase; NAD(P)H, forma reduzida de NAD fosfato; IRES, local de entrada ribossomal interno; GTP, 5′-trifosfato de guanosina; MHC, complexo principal de histocompatibilidade. Crédito: Avanços da Ciência (2025). DOI: 10.1126/sciadv.ady9811
A doença de Alzheimer (DA), principal causa de demência, afeta quase 40 milhões de indivíduos em todo o mundo, resultando numa perda gradual de memória e independência. Apesar da extensa pesquisa nas últimas décadas, não foram encontrados tratamentos que possam interromper ou reverter a progressão desta doença devastadora.
Na DA, um dos principais contribuintes para a disfunção neuronal é a proteína tau. Tau normalmente desempenha um papel crucial em manter a estrutura interna dos neurônios estável, assim como os trilhos dos trens ajudam os trens a permanecerem no curso. No entanto, em algumas doenças, a tau sofre modificações anormais e começa a agregar-se, perturbando este sistema de transporte, levando a danos neuronais e subsequente perda de memória.
Uma equipe internacional de pesquisadores relatou um novo mecanismo pelo qual o aumento do metabólito natural NAD⁺ pode proteger o cérebro da degeneração associada à DA. Seu artigo, intitulado “NAD⁺ reverte os déficits neurológicos de Alzheimer por meio da regulação do splicing alternativo diferencial de RNA de EVA1C”, é publicado em Avanços da Ciência.
A equipa é liderada pelo Professor Associado Evandro Fei Fang da Universidade de Oslo e do Hospital Universitário Akershus, Noruega, em colaboração com o Professor Oscar Junhong Luo da Universidade de Jinan, China, e a Professora Associada Joana M. Silva da Universidade do Minho, Portugal.
Como o NAD⁺ apoia a saúde do cérebro
NAD⁺ (dinucleotídeo de nicotinamida adenina, forma oxidada) é um metabólito vital envolvido no metabolismo energético e na resiliência neuronal do corpo. Normalmente diminui com a idade e especialmente em várias doenças neurodegenerativas.
“Estudos preliminares demonstraram que a suplementação com precursores de NAD⁺, como o ribosídeo de nicotinamida (NR) ou o mononucleotídeo de nicotinamida (NMN), pode oferecer benefícios terapêuticos em modelos animais de DA e em ensaios clínicos iniciais. No entanto, os mecanismos moleculares por trás desses benefícios permanecem em grande parte obscuros”, diz a primeira autora, Alice Ruixue Ai.
O novo estudo revela que o NAD⁺ funciona através de uma via de splicing de RNA anteriormente não identificada. Essa via é regulada por uma proteína chamada EVA1C, que desempenha um papel essencial no processo de splicing do RNA. O splicing de RNA permite que um único gene produza múltiplas isoformas de uma proteína, e uma isoforma pode apresentar efeitos distintos das outras isoformas. A sua desregulação é um dos factores de risco mais recentemente reconhecidos para a DA.
Os pesquisadores descobriram que quando os níveis de NAD⁺ aumentam, o EVA1C ajuda a corrigir erros no splicing do RNA. Este processo de restauração melhora a função de centenas de genes, muitos deles cruciais para a saúde do cérebro, o que pode ajudar a reverter os danos neurodegenerativos causados pela tau.
Validação entre espécies, de vermes a ratos e ao cérebro humano
Para demonstrar o impacto deste mecanismo, os investigadores utilizaram uma abordagem abrangente que incluiu previsões computacionais e validação em diferentes modelos animais, incluindo vermes, ratos, bem como amostras de cérebro humano.
Eles primeiro identificaram mudanças relacionadas à idade no splicing do RNA em um tipo específico de verme. Eles descobriram que a adição de NAD⁺ poderia corrigir os problemas de emenda causados pela proteína tau tóxica. Em camundongos com mutações relacionadas à tau, os suplementos de NAD⁺ melhoraram o splicing do RNA, restauraram a função cerebral e melhoraram o desempenho da memória.
“Notavelmente, descobrimos que quando o gene EVA1C foi derrubado, esses benefícios foram perdidos, confirmando que EVA1C é essencial para a neuroproteção mediada por NAD⁺”, diz o professor associado Evandro Fei Fang-Stavem.
Alinhados com estes estudos em animais, os níveis de EVA1C foram significativamente reduzidos nas células cerebrais de pessoas com DA precoce.
Usando IA para descobrir o mecanismo
Para investigar melhor como o EVA1C funciona, a equipe usou uma plataforma baseada em IA para prever como as proteínas interagem umas com as outras, analisando dados estruturais, sequenciais e evolutivos de milhões de proteínas.
Esta análise revelou que o NAD⁺ promove uma forma específica de EVA1C que se liga eficientemente a proteínas essenciais, que são centrais para o dobramento e depuração de proteínas. Esta conexão liga a homeostase metabólica, os processos de splicing de RNA e o gerenciamento de proteínas, três processos que estão criticamente prejudicados na DA.
Rumo a novos tratamentos para Alzheimer
Ao estabelecer a conexão entre NAD⁺ e EVA1C, este estudo estabelece as bases para o desenvolvimento de novas terapias e otimização de estratégias de aumento de NAD⁺ em humanos.
“Propomos que a manutenção dos níveis de NAD⁺ poderia ajudar a preservar a identidade neuronal e retardar o declínio cognitivo, abrindo caminho para tratamentos combinados para melhorar o splicing do RNA”, diz Ai.
Mais informações:
Ruixue Ai e outros, NAD+reverte os déficits neurológicos de Alzheimer através da regulação do splicing alternativo diferencial de RNA de EVA1C, Avanços da Ciência (2025). DOI: 10.1126/sciadv.ady9811
Citação: NAD⁺ restaura a memória em modelos da doença de Alzheimer corrigindo erros de RNA (2025, 10 de novembro) recuperado em 11 de novembro de 2025 em
Este documento está sujeito a direitos autorais. Além de qualquer negociação justa para fins de estudo ou pesquisa privada, nenhuma parte pode ser reproduzida sem permissão por escrito. O conteúdo é fornecido apenas para fins informativos.
Share this content:

Publicar comentário