Biotics AI, Battlefield 2023, obtém aprovação da FDA para seu produto de ultrassom fetal alimentado por IA
O vencedor do TechCrunch Disrupt Battlefield 2023, Biotics AI, anunciou na segunda-feira que recebeu autorização da FDA para seu software de IA que ajuda a detectar anormalidades fetais em imagens de ultrassom.
O produto foi idealizado pelo CEO fundador Robhy Bustami, que foi criado em uma família de obstetras, incluindo sua mãe, irmã e tio. Ele passou muito tempo em hospitais enquanto crescia, muitas vezes viajando com sua mãe enquanto ela prestava cuidados maternos nos EUA.
Depois de aprender a programar e estudar ciência da computação na UC Irvine, Bustami se uniu a Salam Khan, Chaskin Saroff e Dr. Hisham Elgammal em 2021 para lançar Biotics AI,
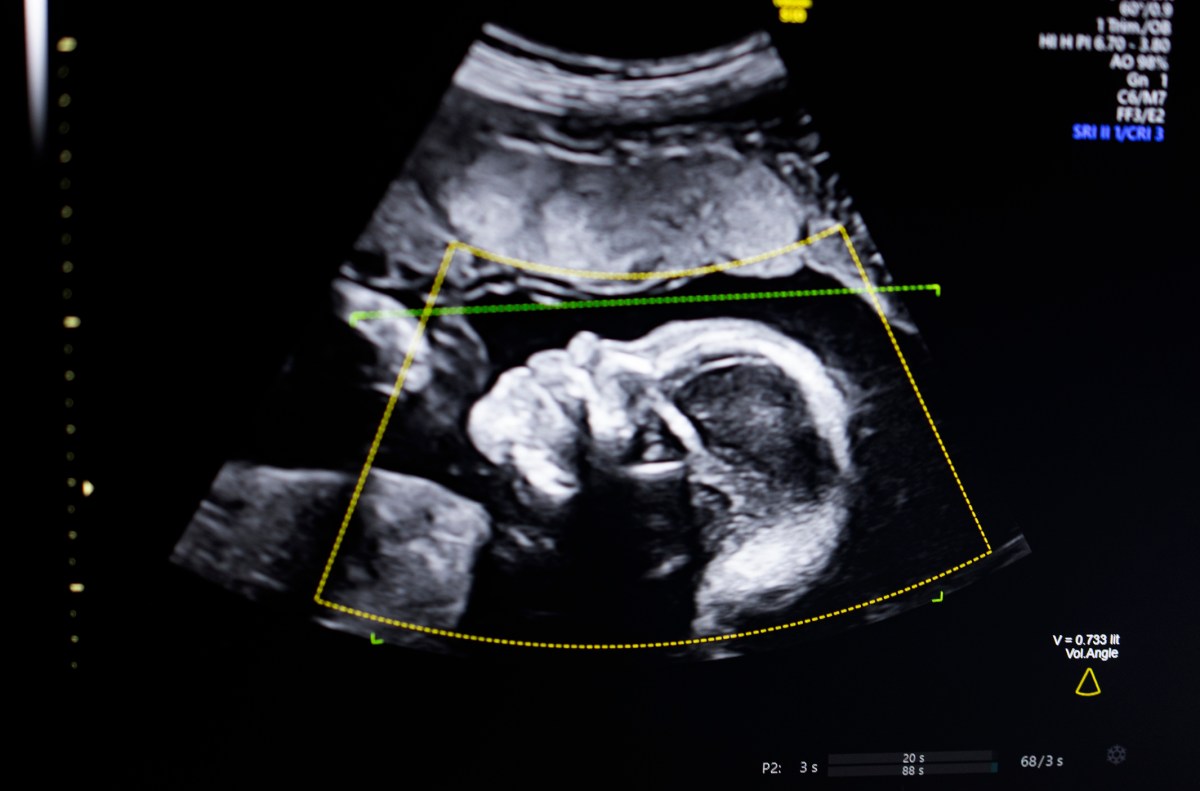
A tecnologia usa IA de visão computacional “para apoiar a avaliação da qualidade do ultrassom fetal, integridade anatômica, relatórios automatizados e integração perfeita em fluxos de trabalho clínicos”, disse Bustami ao TechCrunch.
Ele espera que sua tecnologia ajude os EUA a combater o fato de que os EUA têm um dos piores resultados pré-natais para as mães entre nações de alta renda. As mulheres negras, em particular, enfrentam uma taxa muito elevada de mortes maternas,
Bustami disse que a ultrassonografia pré-natal se tornou a “pedra angular” do monitoramento da gravidez, mas suas imagens de baixa qualidade podem levar a erros de diagnóstico.
Bustami disse que a parte mais difícil não foi construir seus modelos de IA, que foram treinados em um conjunto diversificado de 11.000 ultrassons, mas garantir que a tecnologia funcionasse de maneira confiável no mundo real, especialmente em dados demográficos com maior risco de um resultado trágico.
Evento Techcrunch
São Francisco
|
13 a 15 de outubro de 2026
“Num ambiente onde as disparidades nos resultados dos cuidados de saúde estão bem documentadas, era fundamental demonstrar um desempenho consistente em todos os subgrupos de pacientes, e não apenas em casos idealizados”, continuou Bustami.
O CEO disse que demorou pouco menos de três anos para passar pelo processo da FDA, incluindo testes e validação do produto. A experiência ensinou a ele e sua equipe como é fundamental que o trabalho de engenharia, produto, clínico e regulatório esteja estreitamente alinhado desde o início. “Ao projetar o produto, a validação clínica e o caminho regulatório juntos, em vez de sequencialmente, conseguimos avançar rapidamente”, disse ele.
Agora com a autorização da FDA, Bustami disse que o próximo foco das empresas é expandir-se para vários sistemas de saúde em todo o país. Ele também tem planos de adicionar mais recursos para medicina fetal e saúde reprodutiva.
“Estamos posicionados para dimensionar a distribuição e o impacto clínico, ao mesmo tempo que continuamos a aprofundar o poder da nossa tecnologia”, disse ele.
Share this content:



Publicar comentário